2021-09-30
CSCO学术年会口头汇报丨马建群教授:卡瑞利珠单抗联合紫杉醇和奈达铂新辅助治疗局部晚期食管鳞癌的单臂、II期探索性研究
背景:食管癌是我国癌症患者死亡的主要原因之一,根据世界卫生组织的最新癌症报告,2020年我国新增约32.4万食管癌患者,超过30万人死于食管癌,分别位居全部癌症的第五和第四。针对早期食管癌,内镜黏膜下剥离术(ESD)及外科手术是其主要的治疗方式,而对于中晚期食管癌患者,以外科手术为主的综合治疗则是其主要的治疗方式,但其术后易发生转移,5年生存率仅为50%左右(1)。中晚期食管癌新发病例中约80%的患者在初诊时已经错过了最佳手术治疗时机,仅有20%的患者可直接接受手术治疗,因此针对局部晚期、有潜在手术切除可能的患者,新辅助治疗方案一直是临床专家积极探索的重点。新辅助治疗作为术前治疗方案,不仅能够降低肿瘤分期,消灭亚临床转移灶,还能减少肿瘤种植转移风险,提高手术切除率。术前新辅助治疗主要包括新辅助化疗、新辅助放化疗及新辅助免疫联合治疗等。新辅助化疗疗效有限且毒副作用较大,新辅助放化疗复发率约为30%-40%,临床上需要更有效的围术期全身治疗来应对可见病灶之外的远处转移。因此,新辅助免疫联合治疗的探索是食管癌临床研究的热点。
哈尔滨医科大学附属肿瘤医院马建群教授团队发起的卡瑞利珠单抗联合紫杉醇和奈达铂新辅助治疗局部晚期食管鳞癌的单臂、开发、探索性Ⅱ期临床研究(ESPRIT研究)在2021年CSCO学术年会上发表,并由马建群教授代表研究团队对该研究进行口头汇报。
研究简介:
以根治性手术切除为主的综合治疗是食管癌最主要的治疗方式。对于早期食管癌患者,手术治疗效果较好。而对于局部晚期的食管癌患者,单纯手术治疗的效果有限,术后复发和转移的发生率较高(2)。前期的多项研究提示新辅助化疗有效率偏低,无法达到临床治疗需求,因此,探索更为有效的新辅助治疗方案一直是临床研究重点关注的话题。近年来,免疫治疗在多个瘤种中取得快速突破,在晚期食管癌治疗中已经有多项研究证实了其良好的治疗效果,并已进入CSCO指南推荐,突显出有希望的临床应用前景。
卡瑞利珠单抗是一种人类免疫球蛋白G4(IgG4)单克隆抗体,可与PD-1受体结合,并阻断PD-1/PD-L1通路,激活T细胞,对肿瘤细胞产生免疫杀伤作用(图1)(3)。近年来,有学者提出了传统化疗联合免疫治疗可作为局部晚期和转移性肿瘤的主要治疗模式。研究发现:一方面,化疗引起肿瘤细胞免疫原性死亡,释放肿瘤抗原并可消除癌细胞对免疫系统的抑制;另一方面,肿瘤微环境中的效应T细胞能够通过减弱基底层细胞介导的化疗抵抗增强化疗药物效果,故二者联合应用能够产生“1+1>2”的效果(4)(图2)。目前,卡瑞利珠单抗联合化疗一线治疗食管癌的随机对照Ⅲ期研究(ESCORT-1st)的研究结果已经发表于国际权威医学期刊《美国医学会杂志》(JAMA主刊)(5)。结果显示卡瑞利珠单抗联合紫杉醇和顺铂一线治疗晚期食管癌可显著延长患者的中位总生存(15.3个月 vs. 12.0个月),降低30%的死亡风险, 延长中位无进展生存期(6.9个月vs. 5.6个月),同时提高客观缓解率(72.1% vs. 62.1%)。研究数据极为瞩目,充分证明食管癌化疗联合免疫治疗是大势所趋。
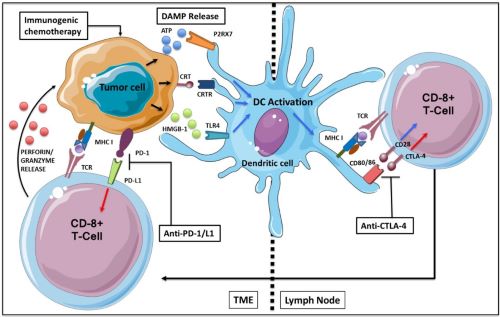
图1. PD-1/PD-L1抗肿瘤的作用通路[4]
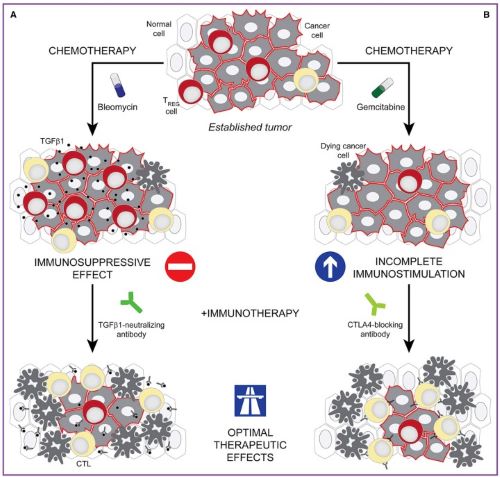
图2. 免疫检查点抑制剂联合化疗的作用机制[5]
ESPRIT研究—卡瑞利珠单抗联合紫杉醇和奈达铂新辅助治疗局部晚期食管鳞癌的阶段性结果已经被2021年CSCO学术年会收录并进行了口头汇报,在会上马建群教授对这项研究的研究设计及阶段性数据进行了详细的介绍。这是一项单臂、前瞻性、Ⅱ期临床研究,计划招募即将进行手术的70例局部晚期食管鳞癌患者。患者将接受2-4个周期的卡瑞利珠单抗(200 mg,iv,q3w),紫杉醇(155 mg/m2,iv,q3w)和奈达铂(80 mg/m2,iv,q3w)。每2个周期进行疗效评价,用药2-4个周期,由研究者团队对患者进行评估,并对可切除的患者进行手术。主要研究终点是病理完全缓解率(pCR),次要研究终点是客观缓解率(ORR)、疾病控制率(DCR)、无病生存期(DFS)、总生存期(OS)、药物的安全性等(图3)。

图3. 研究设计
目前,该项研究已经取得了初步结果。从2020年6月至2021年6月,共有34例符合条件的患者接受了上述新辅助治疗,中位年龄为62岁(47-73岁)。入组的34例患者中,有18例患者进行了疗效评价,其中1例达到完全缓解,8例部分缓解,9例疾病稳定,ORR为50%,DCR为100%,有10例(55.56%)患者在新辅助治疗后实现了降期。另有13例患者未到疗效评价周期,3例脱落。
该研究共13例患者接受手术,其中5例(38.46%)达到pCR,8例(61.5%)达到MPR,8例(61.5%)实现了淋巴结pCR,R0切除率达到100%。所有手术患者的TRG/CAP分级均≤2级,其中5例( 38.46% )患者达到TRG/CAP 0级。治疗药物引起的3/4级不良反应仅有1例,主要是中性粒细胞减少(1/34)。所有患者均可从药物相关毒性中恢复。无吻合口漏且无不良反应导致的治疗延迟事件发生。
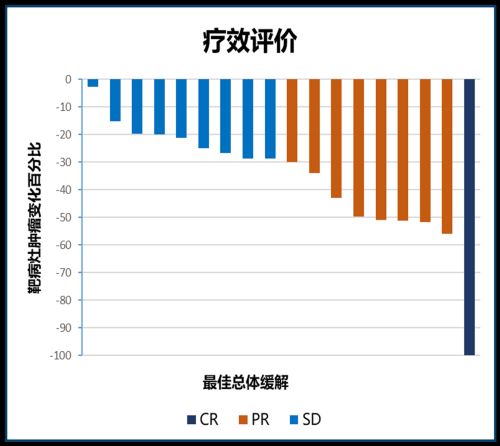
图4. 患者疗效评价瀑布图
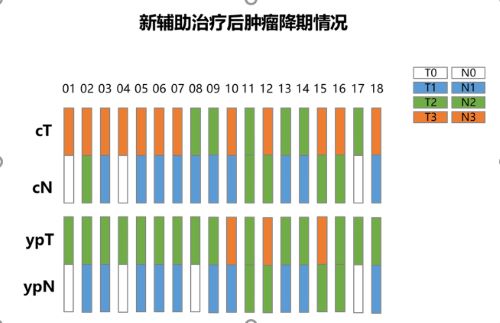
图5. 新辅助治疗后肿瘤降期情况
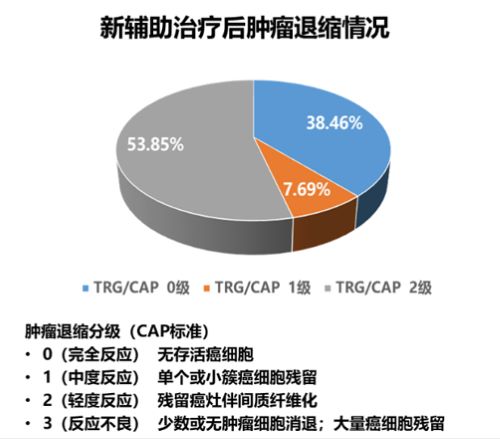
图6. 新辅助治疗后肿瘤退缩情况
在临床实践中,对于局部晚期食管癌患者,常规推荐新辅助放化疗或新辅助化疗。新辅助放化疗的不良反应较大,患者难以耐受,而新辅助化疗的疗效有限,因此限制了其在临床实践中的应用。局部晚期食管癌的新辅助治疗亟需一种行之有效且安全可控的治疗手段。该项研究成果的公布证明了卡瑞利珠单抗联合化疗能够在食管癌新辅助治疗中产生良好的治疗效果,病理完全缓解达到了38.46%,高于其他常规新辅助治疗方案,且安全性可控,发生的3级治疗相关不良事件仅为1例(中性粒细胞减少)。该项研究的结果提示免疫检查点抑制剂联合化疗有望成为可切除局晚期食管癌患者可选择的有效治疗手段。
ESPRIT研究的阶段性数据提示:对于局部晚期可切除的食管癌患者,卡瑞利珠单抗联合紫杉醇和奈达铂的新辅助治疗能够缩小肿瘤并完成降期,38.46%的患者能够达到病理完全缓解,这对于延长患者的生存时间,改善患者的预后是意义重大的。目前这项研究正在持续招募患者中,我们也期待这项研究终期结果的公布能够为食管癌新辅助治疗提供一种新的治疗选择。
参考文献:
1. Siegel RL, Miller KD, Jemal A. Cancer statistics, 2015[J]. CA Cancer J Clin, 2015, 65(1):5-29.
2. 张思维,郑荣寿,左婷婷,等.中国食管癌死亡状况和生存分析[J].中华肿瘤杂志,2016,38(9):709-715.
3. Mathew M, Enzler T, Shu CA, et al. Combining chemotherapy with PD-1 blockade in NSCLC[J]. Pharmacology & therapeutics, 2018, 186: 130-137.
4. Galluzzi L, Buque A, Kepp O, et al. Immunological effects of conventional chemotherapy and targeted anticancer agents[J]. Cancer cell, 2015, 28(6): 690-714.
5. Luo H, Lu J, Bai Y, et al. Effect of Camrelizumab vs Placebo Added to Chemotherapy on Survival and Progression-Free Survival in Patients With Advanced or Metastatic Esophageal Squamous Cell Carcinoma: The ESCORT-1st Randomized Clinical Trial[J]. JAMA, 2021, 326(10): 916-925.