2025-06-10
2025 ASCO快速口头报告︱恒瑞创新药阿得贝利单抗联合治疗三阴性乳腺癌脑转移研究结果披露
2025年美国临床肿瘤学会(ASCO)年会于当地时间5月30日至6月3日在芝加哥盛大举行。本次大会上,由复旦大学附属肿瘤医院胡夕春教授和张剑教授牵头开展的“阿得贝利单抗联合贝伐珠单抗和顺铂/卡铂治疗三阴性乳腺癌脑转移患者的II期临床研究(ABC研究)”研究在快速口头报告专场进行了汇报[1]。阿得贝利单抗联合贝伐珠单抗和顺铂/卡铂有望为晚期三阴性乳腺癌脑转移患者提供新的联合治疗方案。

2025 ASCO现场图:复旦大学附属肿瘤医院李婷教授进行口头报告
01研究背景
乳腺癌是女性最常见的恶性肿瘤,是仅次于肺癌易发生脑转移的第二常见实体瘤,初诊时有5%的患者发生脑转移,进展中15%~30%的患者会发生脑转移[2]。其中三阴性乳腺癌(TNBC)患者发生脑转移时间早、发生率高,在晚期TNBC中脑转移发生率为26%~46%[2-3]。
既往报道显示PD-1/PD-L1抑制剂、含铂化疗方案和贝伐珠单抗可能有效治疗脑转移[4-7]。本研究探索了阿得贝利单抗(PD-L1抑制剂)联合贝伐珠单抗和顺铂/卡铂治疗TNBC伴脑转移患者的疗效及安全性。
02研究设计
本研究为单中心、单臂Ⅱ期临床试验,共纳入35例复发转移三阴性乳腺癌脑转移患者,既往未接受过贝伐珠单抗和PD-1/PD-L1抑制剂治疗。符合条件受试者接受阿得贝利单抗(20mg/kg)联合贝伐珠单抗(7.5mg/kg)和顺铂(75mg/m2)或卡铂(AUC=5)治疗,治疗至疾病进展或不可耐受。
研究主要终点为根据RANO-BM标准评估的中枢神经系统客观缓解率(CNS-ORR),次要终点包括中枢神经系统临床获益率(CNS-CBR)、无进展生存期(PFS)、总生存期(OS)、首次进展位置及安全性。
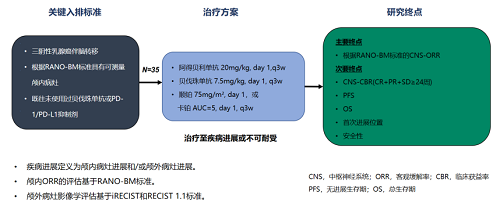
研究设计
03研究结果
截至2025年4月10日,在所有患者中,42.9%(15例)入组时已有神经系统症状,80.0%(28例)既往未接受任何脑转移的局部治疗。患者中位既往治疗线数为2线(范围0–4),其中40%(14例)既往接受过铂类药物。
中位随访时间为17.5个月,确认的CNS-ORR为77.1%(27/35),确认的CNS-CBR为80%(28/35),CNS-PFS为11.5个月(6.2-NR),整体mPFS为8.3个月(5.8-11.5),中位OS尚不成熟。
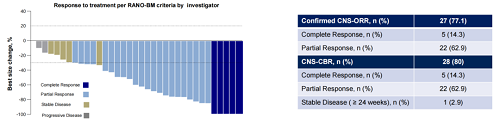
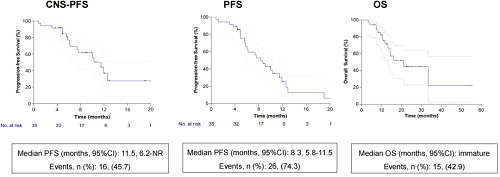
PFS和OS结果
亚组分析显示,在PD-L1阴性(CPS<1)人群中,CNS-PFS为11.5个月,在PD-L1阳性(CPS≥1)人群中,CNS-PFS由于事件数较少尚未达到;整体PFS在PD-L1阴性和阳性人群中分别为7.6个月和10个月。
本研究引入了三阴性乳腺癌“复旦分型”,根据分型显示,在免疫调节型(IM型)中,CNS-PFS尚未达到,在非免疫调节型(Non-IM型)中,CNS-PFS为10个月;整体PFS在免疫调节型(IM型)和非免疫调节型(Non-IM型)展示出明显差异,PFS分别为19个月和6.1个月。
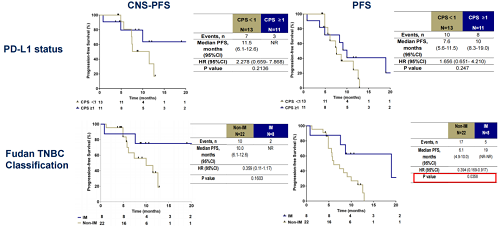
亚组结果
在安全性方面,此方案整体可控。
04研究结论
阿得贝利单抗联合贝伐珠单抗和顺铂/卡铂治疗是首个在伴有脑转移的TNBC中显示出高颅内抗肿瘤活性、延长CNS-PFS和PFS的治疗方案,且此方案安全性良好,有望为晚期三阴性乳腺癌脑转移患者提供新的联合治疗方案。研究提示PD-L1状态和TNBC“复旦分型”可能预测此联合治疗的疗效,未来需开展相关研究来进一步验证。
参考文献:
1.A phase II clinical study of adebrelimab and bevacizumab combined with cisplatin/carboplatin in triple-negative breast cancer patients with brain metastases. ASCO 2025:Rapid Oral abstract 1018.
2.Niwinska A, et al. Cancers, 2022, 14(4): 965.
3. Venkitaraman R, et al. Clin Oncol, 2009, 21(9): 729-730.
4. Ilana S, et al. The oncologist, 2022, 27(7): 538-547.
5. Amelie G, et al. Breast Cancer Res. 2020 Oct 23;22(1):111.
6. Miao L, et al. Oncology letters, 2013, 5(3): 983-991.
7. Caroline B, et al. Br J Cancer, 2021, 124(1): 142-155.