2026-05-06
恒瑞创新药海曲泊帕治疗儿童和青少年原发免疫性血小板减少症III期研究数据荣登JHO
近日,恒瑞医药自主研发的新型口服血小板生成素受体激动剂(TPO-RA)海曲泊帕在6-17岁儿童和青少年原发免疫性血小板减少症(ITP)患者的III期临床数据,发布于血液顶级期刊《血液学与肿瘤学》(Journal of Hematology & Oncology,简称JHO,IF:40.4)[1]。本研究由首都医科大学附属北京儿童医院王天有教授、吴润晖教授牵头,是一项全国17家中心参研的多中心、随机、双盲、安慰剂对照III期临床试验。研究首次证实了海曲泊帕在6-17岁儿童和青少年ITP患者中的疗效与安全性,有望为此类患者二线治疗提供新的口服选择[1]。

研究发表于Journal of Hematology & Oncology
01 研究背景
ITP是儿童最常见的获得性出血性疾病[2],以免疫介导的血小板破坏增加和生成不足为特征,年发病率达1.6-5.3/10万,且随年龄增长慢性化风险升高,10岁以上患儿慢性化率可达47%[3,4]。目前儿童ITP的治疗目标以维持安全血小板计数、预防出血为主,一线治疗以糖皮质激素、静脉免疫球蛋白(IVIg)为主,但部分患儿对一线治疗反应不佳或出现复发,需依赖二线治疗。
TPO-RAs类药物已成为ITP二线治疗的核心选择,但现有药物仍存在局限。海曲泊帕作为新型口服TPO-RA,已于2021年获批用于既往对糖皮质激素、免疫球蛋白等治疗反应不佳的慢性原发ITP成人患者的治疗,但其在儿科人群中的疗效与安全性尚未明确,亟需高质量临床研究验证。
02 研究设计
该研究为III期临床试验(NCT04737850),88例6-17岁中国ITP患儿按2:1随机分为海曲泊帕组(n=57)和安慰剂组(n=31),研究设计如下:
● 研究人群:纳入确诊ITP≥6个月、血小板计数持续<30×10⁹/L,且对至少1种一线治疗反应不佳或复发的患儿,基线特征在两组间均衡可比。
● 治疗方案:双盲期(12周)内,海曲泊帕组给予每日1次口服海曲泊帕(初始剂量2.5mg/日),安慰剂组给予匹配安慰剂;随后进入12周开放标签延伸期,安慰剂组交叉至海曲泊帕治疗,剂量可根据血小板计数调整(最大7.5mg/日)。
● 核心终点:主要终点为第10周血小板计数≥50×10⁹/L的患者比例;关键次要终点为第5-12周内血小板计数≥50×10⁹/L且维持≥6周、无需补救治疗的持续应答率。
● 安全性评估:全程监测不良事件(AE)、实验室检查(肝酶、心电图等),重点关注TPO-RAs类药物相关的特殊不良事件(肝功能异常、血栓、白内障等)。
03 研究结果
1 主要终点:短期疗效显著优于安慰剂
第10周时,海曲泊帕组61.4%(35/57)的患儿达到血小板计数≥50×10⁹/L,而安慰剂组仅为9.7%(3/31),组间率差为52.7%(95% CI:35.9-69.5,P<0.0001),证实了海曲泊帕可显著提升儿童和青少年ITP患者的血小板应答率。
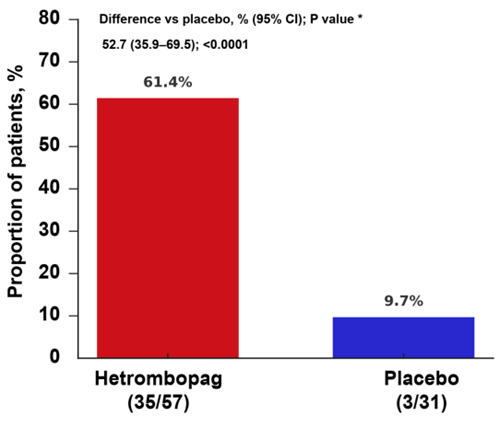
图1. 海曲泊帕组和安慰剂组第10周血小板应答率
2 关键次要终点:持续应答率突出
第5-12周内,海曲泊帕组43.9%(25/57)的患儿实现持续应答,安慰剂组患儿均未达到持续应答(组间率差为43.7%,95% CI:28.5-58.9,P<0.0001)。这一持续应答率与其他口服TPO-RAs在儿童ITP人群中的表现一致,验证了海曲泊帕持久升板的能力。
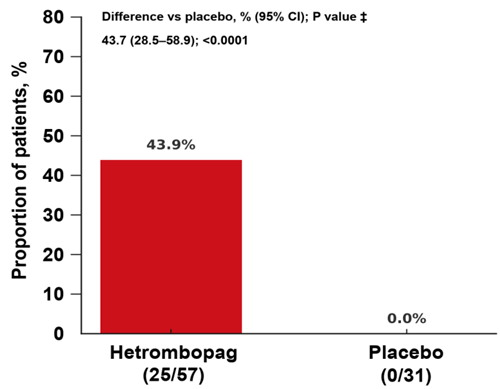
图2. 海曲泊帕组和安慰剂组持续应答率
3 次要终点:多维度验证治疗获益
● 至少1次达到血小板应答的比例:海曲泊帕组91.2%,安慰剂组64.5%(P=0.0033);
● 起效速度:海曲泊帕组中位首次应答时间仅20.0天,显著快于安慰剂组的43.0天。
● 补救治疗需求:海曲泊帕组仅21.1%需使用IVIg或血小板输注,安慰剂组达45.2%;
● 出血改善:海曲泊帕组基线出血发生率59.6%,第12周降至15.8%,而安慰剂组仍维持在48.4%。
4 长期疗效:24周中位总应答时间达85天
24周内,海曲泊帕组26.3%的患儿在≥75%的随访时间点维持血小板应答,中位最大持续应答时间44.5天,中位总应答时间85.0天。
5 安全性
研究证实,海曲泊帕在儿童和青少年ITP患者中的安全性与安慰剂相当,无新增安全信号,且全程未观察到QT间期延长、血栓栓塞、骨髓纤维化、克隆演变等TPO-RAs相关高关注不良事件。
04 总结
此项III期临床试验证实,对一线治疗反应不佳或复发的6-17岁ITP患儿,每日一次口服海曲泊帕(初始剂量2.5mg),可显著提升血小板计数,减少出血事件和补救治疗需求,且24周持续升板,整体安全性良好,有望为儿科ITP二线治疗新增一种新的口服选择。海曲泊帕用于既往对糖皮质激素、免疫球蛋白等治疗反应不佳的原发免疫性血小板减少症(ITP)≥6岁的儿童患者的上市许可申请已于2025年8月获国家药监局受理。
参考文献:
[1]. Wu et al. Efficacy and safety of hetrombopag, a novel thrombopoietin receptor agonist, in children and adolescents with immune thrombocytopenia: results from a randomized, multicenter, placebo-controlled phase 3 trial. J Hematol Oncol. 2026;19:24
[2].Al-Jadiry M, Ghali H, Aref I, et al. PB2301: PEDIATRIC IMMUNE THROMBOCYTOPENIA; A GLANCE AT PATIENTS AND URRENT THERAPEUTIC CHALLENGES. HemaSphere 6(Suppl) 2020.
[3]. Working Group of Chinese Guideline for the Diagnosis and Treatment of Childhood Primary Immune Thrombocytopenia; Subspecialty Group of 2.Hematologic Diseases, Society of Pediatrics, Chinese Medical Association; Editorial Board, Chinese Journal of Pediatrics. Adapted guideline for the diagnosis and treatment of primary immune thrombocytopenia for Chinese children (2021). Pediatr Investig. 2022;6(2):63–74.
[4]. Kühne T, Buchanan GR, Zimmerman S, et al. A prospective comparative study of 2540 infants and children with newly diagnosed idiopathic thrombocytopenic purpura (ITP) from the Intercontinental Childhood ITP Study Group. J Pediatr. 2003;143(5):605–8.
声明:
1.本新闻旨在分享学术前沿动态,仅供医疗卫生专业人士基于学术目的参阅,非广告用途。
2.恒瑞医药不对任何药品和/或适应症作推荐。
3.本新闻中涉及的信息仅供参考,请遵从医生或其他医疗卫生专业人士的意见或指导。医疗卫生专业人士作出的任何与治疗有关的决定应根据患者的具体情况并遵照药品说明书。